
Introduction > Dossiers > Liaisons Hydrogènes
Liaisons Hydrogènes
Les liaisons hydrogènes ( ou ponts hydrogènes ) sont des liaisons intermoléculaires entre un atome d'hydrogène et un atome électronégatif d'une autre molécule. C'est une interaction de type électrostatique.

Explications :
Lorsqu'un atome d'hydrogène est lié par une liaison covalente ( liaisons habituelles entre atome au seins d'une molécule ) à un autre atome il peut être attiré par un troisième atome. Mais il faut que l'atome de sa liaison covalente soit très électronégatif ( il s'agit généralement d'atomes d'azote N, d'oxygène O, de fluor F ou de chlore Cl ) : dans ce cas les électrons de cette liaison seront attirés vers l'atome électronégatif et l'atome d'hydrogène se dotera donc d'une charge partielle positive  ( Voir polarité ). Cette charge partielle positive peut être attirée par une autre charge partielle négative. Le pont hydrogène résulte donc de l'attraction qui s'exerce entre la charge partielle positive de l'hydrogène et la charge partielle négative d'un autre atome.
( Voir polarité ). Cette charge partielle positive peut être attirée par une autre charge partielle négative. Le pont hydrogène résulte donc de l'attraction qui s'exerce entre la charge partielle positive de l'hydrogène et la charge partielle négative d'un autre atome.
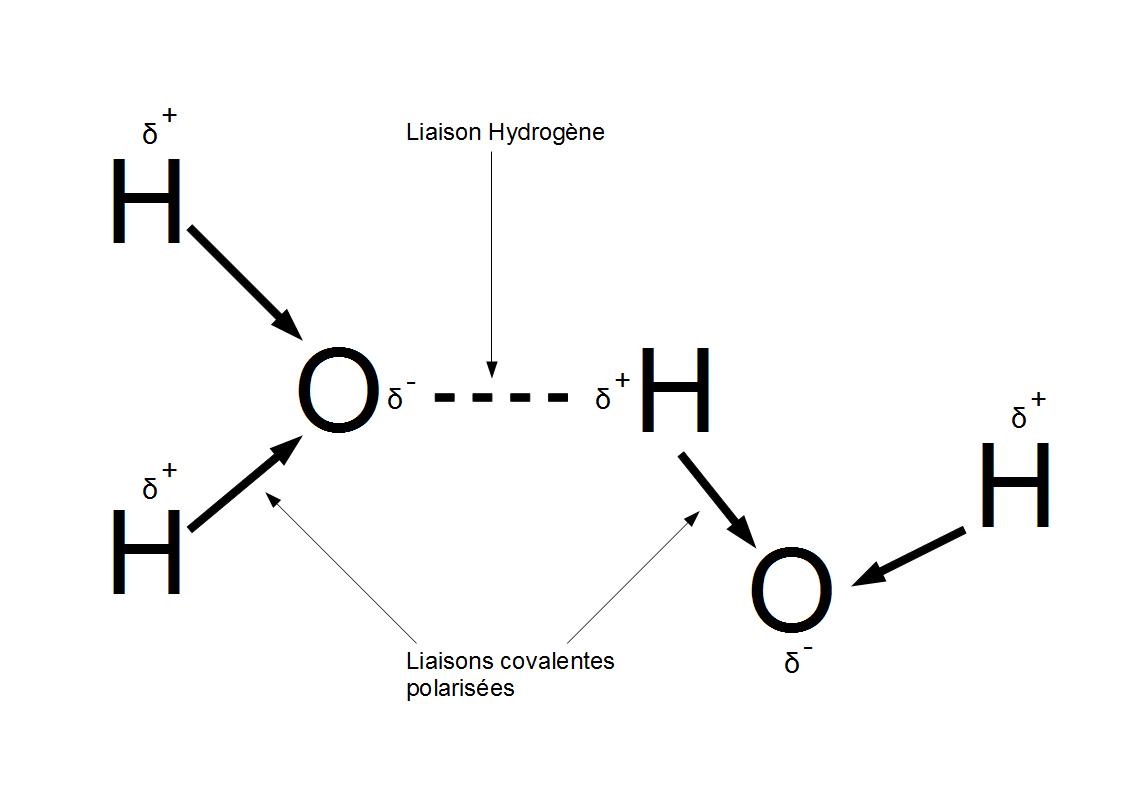
Particularités :
On observe des liaisons hydrogènes au seins de l'eau entre les hydrogènes des molécules d'eau et les oxygènes d'autres molécules d'eau.
Ces liaisons changent en fonction de la température ce qui explique la capacité particulière de l'eau à occuper moins d'espace à l'état liquide qu'à l'état solide. La glace est donc moins dense et flotte sur l'eau contrairement à la plupart des matériaux.
Les atomes d'un ponts hydrogènes respectent une certaine directionnalité ce qui crée une certaine architecture au seins d'une succession de liaisons hydrogènes. C'est cette architecture qui donne à la glace sa forme de cristaux.
Touts les groupes carbonyles C=O sont capables de créer ces liaisons.
Les liaisons H maintiennent la forme d'hélice de l'ADN. Elles sont aussi responsables de la structure secondaire des protéines, notamment de l'hélice alpha et du feuillet beta. Elles jouent donc un rôle très important dans la vie.
Les liaisons hydrogènes ont la capacité de transférer des ions H+ d'une molécule à une autre : c'est ce qui crée la réactivité des milieux aqueux et donc qui permet à la vie de s'y développer. Sans ces liaisons, la vie ne pourrait certainement pas se développer dans l'eau.
Ces liaisons donnent au Kevlar son incroyable capacité de résistance